Mülheimer Forscher lösen ein weiteres Rätsel der Photosynthese
Die hohe Effizienz des natürlich Wasserspaltungskatalysators könnte durch eine chemische Isomerisierungsreaktion erklärt werden
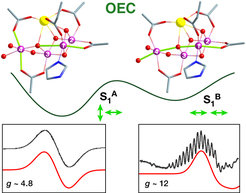
Zwei Isomere des wasseroxidierenden Katalysators entstammen den unterschiedlichen Verzerrungen entlang alternativer „Jahn-Teller“ Achsen. Diese von Pantazis und Koautoren mit Hilfe von Quantenchemie und EPR Spektroskopie entdeckte strukturelle Heterogenität führt zu einer bisher nie charakterisierten mechanistischen Vielfalt.
“Grüner” Wasserstoff wird häufig als das “Petroleum von Morgen” bezeichnet. Um eine klimaneutrale Versorgung mit Brennstoffen zu gewährleisten, muss die Energieindustrie von Kohlenstoff basierten Brennstoffen auf „Solar fuels“ umstellen, welche mit Hilfe von Sonnenlicht im Rahmen einer artifiziellen Photosynthese gewonnen werden. Ein Baustein auf dem langen und komplizierten Weg zu dieser Umstellung, ist ein präzises Verständnis der Chemie im innersten Zentrum der biologischen Photosynthese. Die Forschungsgruppe um Dr. Dimitrios Pantazis am Max-Planck Institut für Kohlenforschung leistet in dem Bereich der photosynthetischen Wasseroxidation bereits seit Jahren bahnbrechende Beiträge.
Gemeinsam mit internationalen Kooperationspartnern hat das Team nun eine neuartige Reaktion im aktiven Zentrum des wasseroxidierenden Katalysators (dem „Oxygen Evolving Complex“, OEC) entdeckt, welche neues Licht auf den Reaktionsmechanismus dieser biochemisch zentral wichtigen Reaktion wirft. Die Entdeckung dreht sich um eine neuartige „Isomerisierungsreaktion“, bei welcher chemische Bindungen innerhalb eines Moleküls gebrochen und in anderer Form neu geknüpft werden. Die entstehende Verbindung bezeichnet man dann als ein „Isomer“ der Ausgangsverbindung.
Isomere treiben parallele Reaktionsschritte in der biologischen Wasseroxidation
Die in der Zeitschrift “Angewandte Chemie“ erschienene Publikation von Pantazis und Koautoren benutzt modernste quantenchemische Methoden in Kombination mit anspruchsvollen magnetischen Messmethoden („Electron Paramagnetic Resonance“, EPR, Spektroskopie), um strukturelle Einblicke in die Reaktionsintermediate der Wasseroxidation zu erhalten. Die Analyse der Daten legt nahe, dass bereits im Ausgangszustand des Enzymes (dem „resting state“ oder auch „S1 State“ genannt) zwei Isomere des Katalysators vorliegen, welche die Forscher als „Jahn-Teller Orientierungs-Isomere“ bezeichnet haben. Dieser Effekt führt dazu, dass die im aktiven Zentrum der Photosynthese enthaltenen Manganionen in unterschiedlichen Richtungen Verzerrungen ihrer Koordinationssphäre erleiden können, welche zu der beobachteten strukturellen Vielfalt führen.
Diese Beobachtung ist insofern von höchster Bedeutung, als dass die verschiedenen Isomere im Ausgangszustand, in der logischen Konsequenz auch zu unterschiedlichen Reaktionspfaden im weiteren Verlauf der Reaktion führen müssen – eine Option, die bisher noch nie in der Literatur diskutiert wurde. Das wiederum bedeutet, dass es in der natürlichen Photosynthese nicht einen, sondern mindestens zwei unterschiedliche Reaktionsmechanismen gibt, welche parallel zueinander ablaufen. Diese mechanistische Vielfalt, so Dr. Pantazis, könnte zu der enormen Effizienz und Selektivität beitragen, mit welcher die Natur diese zentrale biochemische Reaktion ausführt. Diese unerwarteten Ergebnisse lüften nicht nur ein weiteres Geheimnis der Photosynthese, sondern geben Anlass zu einer Vielzahl von neuen Fragen, welche die Photosyntheseforschung in den kommenden Jahren beflügeln wird.
Die Arbeit “Orientational Jahn–Teller Isomerism in the Dark-Stable State of Nature’s Water Oxidase” ist in der Zeitschrift „Angewandte Chemie“ erschienen.
Publication: M. Drosou, G. Zahariou, D. A. Pantazis. “Orientational Jahn–Teller Isomerism in the Dark-Stable State of Nature’s Water Oxidase”, Angew. Chem. Int. Ed. (2021) https://doi.org/10.1002/anie.202103425






